Comunicado. AbbVie anunció que el segundo concurso anual AbbVie Migraine Career Catalyst Award ya acepta inscripciones. La compañía se enorgullece de continuar esta iniciativa nacional que apoya a las personas con migraña, premiando a 20 participantes, quienes podrán utilizar para alcanzar sus metas personales, profesionales y educativas.
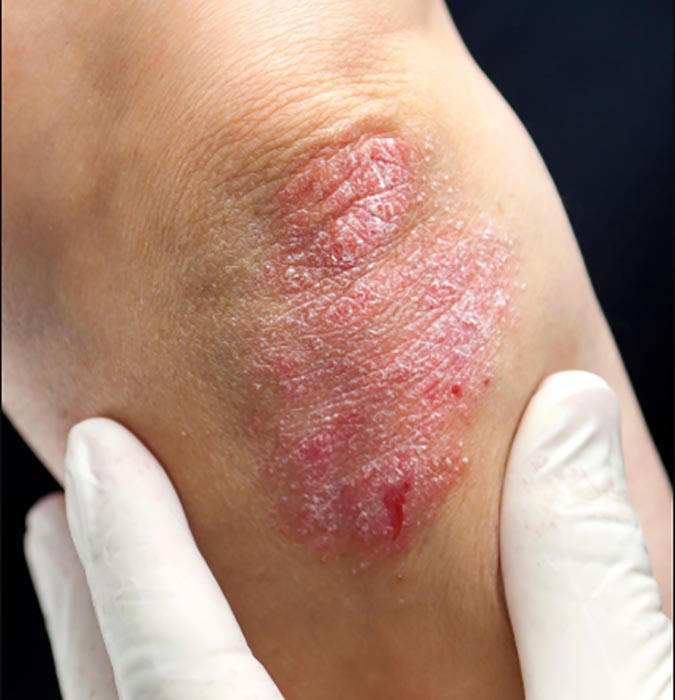
La migraña es la segunda causa principal de discapacidad a nivel mundial. Con síntomas como fuertes dolores de cabeza, náuseas y sensibilidad a la luz, que a menudo interrumpen las actividades cotidianas, dificultando un rendimiento constante en el trabajo o la escuela. Casi el 90% de la pérdida de productividad relacionada con la migraña ocurre mientras las personas continúan trabajando a pesar de los síntomas. En un estudio de AbbVie, más de la mitad de las personas con migraña crónica, una forma de migraña caracterizada por dolores de cabeza durante 15 o más días al mes, informaron que la enfermedad había afectado negativamente su carrera profesional. Estos hallazgos subrayan la importancia de cómo la concienciación sobre la migraña en todas sus formas puede ayudar a reducir el estigma y fomentar una mayor comprensión de cómo afecta a los colegas en el lugar de trabajo.
“La migraña puede generar desafíos significativos en el ámbito laboral que pueden limitar las oportunidades profesionales y el crecimiento. Como parte de nuestro compromiso continuo con quienes viven con migraña, nos complace continuar con el concurso AbbVie Migraine Career Catalyst Award por segundo año consecutivo. Nuestro objetivo es ir más allá del tratamiento y brindar un apoyo significativo que empodere a las personas para avanzar con confianza”, afirmó Jag Dosanjh, vicepresidente sénior de AbbVie y presidente de Neurociencia y Oftalmología.
El año pasado, 20 ganadores de diversos orígenes profesionales utilizaron el premio para tomar medidas prácticas para alcanzar sus objetivos, ya sea crear una oficina en casa adaptada a las personas con migraña, ampliar sus redes profesionales en conferencias o perfeccionar sus habilidades a través de oportunidades de desarrollo.
Hoy también publicamos las siguientes notas y más...
Almirall inicia un cambio de paradigma hacia una atención holística al paciente en dermatología
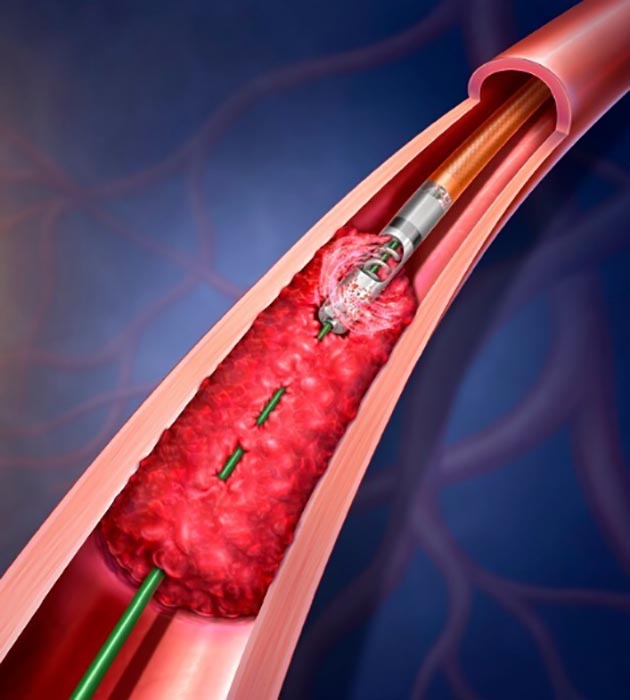
FDA aprueba dispositivo de Abbott que reemplaza la válvula mitral sin cirugía a corazón abierto