Comunicado. La farmacéutica anunció una inversión de 50 mil mdd Estados Unidos durante los próximos cinco años. Estas inversiones refuerzan la ya significativa presencia de Roche en dicho país, con 13 centros de fabricación y 15 de I+D en las divisiones farmacéutica y de diagnóstico, y se prevé que generen más de 12 mil nuevos empleos, incluyendo casi 6,500 en construcción, así como 1,000 en instalaciones nuevas y ampliadas.
Como parte de esta inversión, Roche ampliará su presencia actual de más de 25 mil empleados en 24 centros de ocho estados de Estados Unidos. La inversión incluirá:
- Ampliación y mejora de sus capacidades de fabricación y distribución en Estados Unidos para su innovadora cartera de medicamentos y diagnósticos en Kentucky, Indiana, Nueva Jersey, Oregón y California.
- Una instalación de fabricación de terapia genética de última generación en Pensilvania
Un nuevo centro de fabricación de 900 mil pies cuadrados para respaldar la creciente cartera de medicamentos de última generación para bajar de peso de Roche (la ubicación se anunciará próximamente)
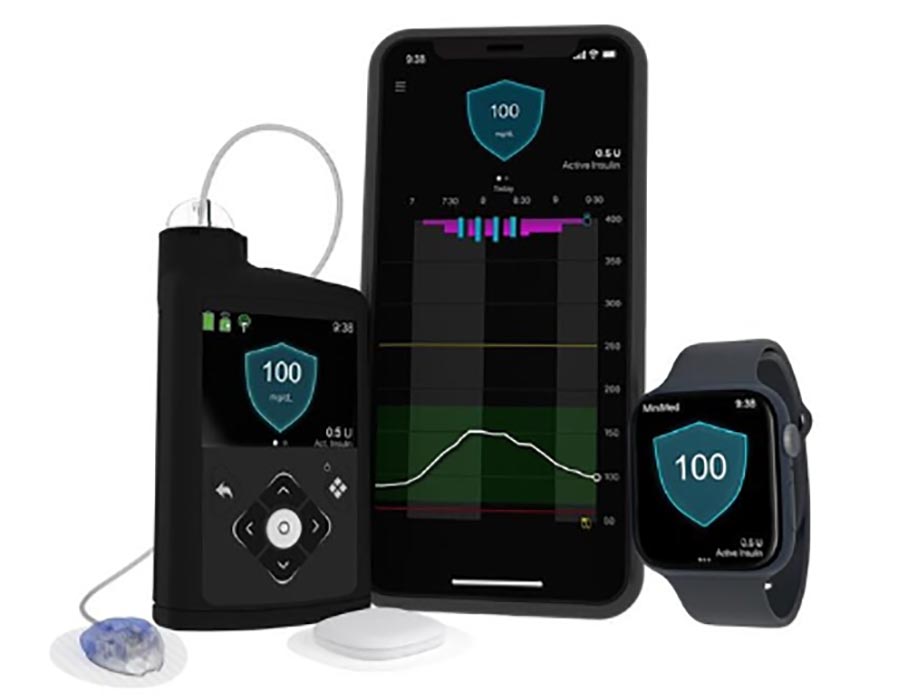
- Una nueva planta de fabricación para la monitorización continua de la glucosa en Indiana
- Un nuevo centro de I+D en Massachusetts, que realiza investigaciones de inteligencia artificial (IA) de vanguardia y sirve como centro para nuestros nuevos esfuerzos de investigación y desarrollo cardiovascular, renal y metabólico.
- Ampliación y modernización significativa de nuestros centros de investigación y desarrollo de productos farmacéuticos y de diagnóstico existentes en Arizona, Indiana y California
“Roche es una empresa suiza con una sólida trayectoria en más de 130 países de todo el mundo. Las inversiones anunciadas hoy subrayan nuestro compromiso a largo plazo con la investigación, el desarrollo y la fabricación en Estados Unidos. Nos enorgullecemos de nuestros 110 años de experiencia en Estados Unidos, que han sido un motor clave para el empleo, la innovación y la creación de propiedad intelectual en el país, tanto en nuestras divisiones farmacéutica como de diagnóstico. Nuestras inversiones de 50 000 millones de dólares estadounidenses durante los próximos cinco años sentarán las bases de nuestra próxima era de innovación y crecimiento, que beneficiará a los pacientes de Estados Unidos y de todo el mundo”, declaró Thomas Schinecker, director ejecutivo del Grupo Roche.
Una vez que toda la nueva y ampliada capacidad de fabricación entre en funcionamiento, Roche exportará más medicamentos desde Estados Unidos de los que importa. Hoy, su división de diagnóstico ya cuenta con un superávit de exportación del país norteamericano a otros países.
Hoy también publicamos las siguientes notas y más...
FDA aprueba a Medtronic integrar su bomba de insulina con el sensor Simplera Sync